司普奇拜單抗多項臨床研究成果亮相2024 EADV大會
公司要聞
?2024年09月28日
2024年9月25日-28日,第33屆歐洲皮膚病與性病學會(2024 EADV)年會于荷蘭阿姆斯特丹召開,康諾亞自主研發的首個國產新型IL-4Rα抗體藥物司普奇拜單抗的系列研究數據,以口頭報告和電子壁報的形式亮相大會,進一步展示司普奇拜單抗在治療成人中重度特應性皮炎(AD)上的優勢和潛力。
在本屆大會上,北京大學人民醫院張建中教授以Oral Presentation形式,報告了司普奇拜單抗III期臨床研究的52周長期隨訪結果。52周隨訪數據體現了司普奇拜單抗對患者報告結局(PROs)的影響,顯示出其對AD患者報告結局的持續有效改善,可助力達標治療長期目標的達成,幫助廣大AD患者重獲健康自信。
圖:張建中教授在EADV大會進行口頭報告
52周隨訪數據顯示:
01
首劑即可起效、持續緩解瘙癢
司普奇拜單抗首劑治療僅1天后,每日PP-NRS較基線變化率即顯著優于安慰劑,快速緩解瘙癢(圖1A),(P<0.001)。
隨司普奇拜單抗的持續治療,患者瘙癢可以得到持續有效的控制,至第52周,司普奇拜單抗單藥治療組每日PP-NRS評分周平均值≤4的患者比例高達84.9%(圖1B)。
至第52周,司普奇拜單抗單藥治療組35.2%患者達到每日PP-NRS評分周平均值≤1,達瘙癢控制更高目標,實現無癢緩解(圖1C)。
司普奇拜單抗治療52周后停藥8周內,依然可獲得良好的瘙癢控制,停藥第8周僅5.7%的患者出現瘙癢惡化或失效(圖1D)。
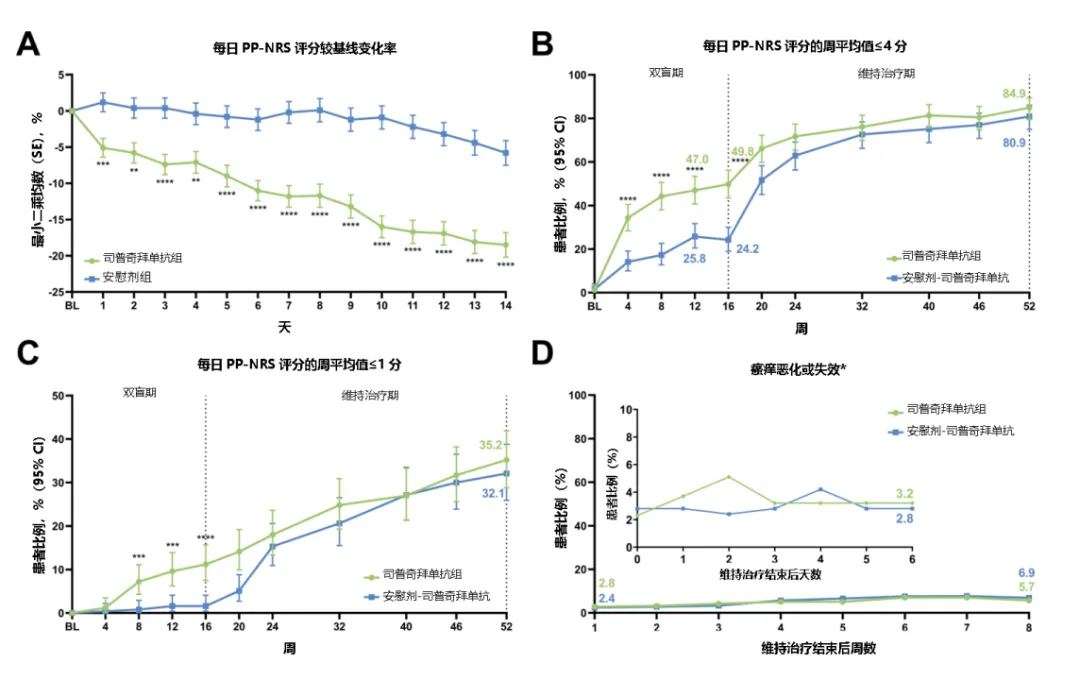
圖1 司普奇拜單抗快速、持續改善AD患者瘙癢
*瘙癢失效定義為第52周時PP-NRS評分周平均值較基線改善≥4分,維持治療結束后PP-NRS評分較基線改善<4分。瘙癢惡化定義為第52周時PP-NRS評分周平均值≤6分,維持治療結束后PP-NRS評分周平均值升高≥4分。
02
改善生活質量,安穩助力達標
司普奇拜單抗可顯著并持續改善DLQI和POEM評分,提高生活質量(圖2A-B)。維持治療期,至第52周,司普奇拜單抗單藥治療組DLQI評分≤5、POEM評分≤7的患者比例均高達約70%(圖2C-D)。司普奇拜單抗長期治療可持續改善患者生活質量,提高患者的臨床獲益。
此外,在本次大會中,司普奇拜單抗還公布了III期臨床研究的一項事后分析結果,評估了司普奇拜單抗在初始不同應答水平患者中繼續治療的長期療效,以期為該款藥物的臨床應用提供更完備的指導,研究結果顯示:
03
無論初始應答水平如何,司普奇拜單抗長期治療均可獲得持續有效改善
維持治療期間,治療16周應答的患者繼續使用司普奇拜單抗治療36周均可保持較高的EASI-75以及IGA應答率(圖3A-B)。
停藥后僅1位患者(0.9%)在第60周復發(定義為EASI評分較基線下降<50%且IGA評分≥2)。
治療16周未達應答標準的患者中,繼續治療36周依然可獲得高水平的EASI-75以及IGA應答率(圖3A-B)。
同時,初始治療應答以及無應答的患者,繼續治療36周,均可持續改善PP-NRS較基線改善≥4分應答率(圖3C),提示無論患者初始應答水平如何,司普奇拜單抗均可持續改善皮損,緩解瘙癢。
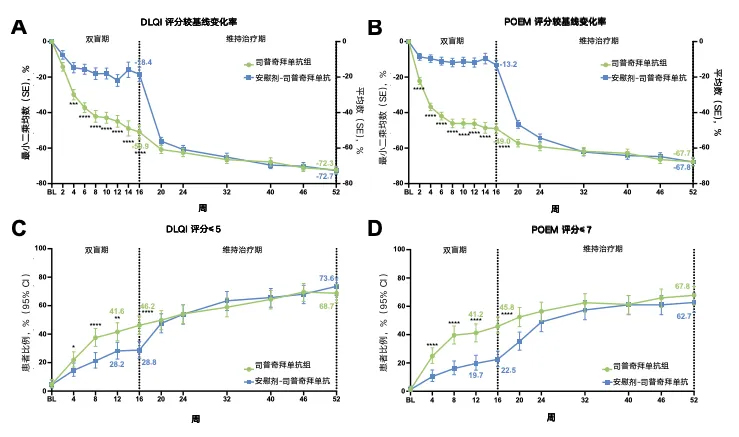
圖3 應答者和無應答者52周隨訪結果
康悅達®(司普奇拜單抗)于2024年9月12日宣布獲得國家藥品監督管理局批準上市,用于治療成人中重度特應性皮炎。該產品是首個國內自主研發并獲批上市的針對IL-4Rα抗體藥物,填補了國產特應性皮炎生物制劑領域的空白,為患者帶來達成EASI-90更高治療目標的新方案。目前康悅達®(司普奇拜單抗)已在全國多地實現處方落地,正式進入臨床應用,惠及廣大患者。
