CMG901 I期臨床研究數據最新結果在ASCO Plenary Series以口頭報告形式公布
公司要聞
?2023年11月08日
KYM901研究(NCT04805307)的目的是評價CMG901在晚期實體瘤受試者中的安全性和耐受性、藥代動力學特征、免疫原性及初步有效性。截至2023年7月24日,2.2mg/kg、2.6mg/kg、3.0mg/kg三個劑量組共納入113例胃癌╱胃食管結合部腺癌患者(分別為44、50、19例)。所有受試者均接受了至少一線的標準治療(既往中位治療線數為2線),74%的受試者既往接受過抗PD-1/PD-L1治療。
安全性方面,與藥物有關的≥3級治療期間出現的不良事件發生率為54%,與藥物有關的嚴重不良事件發生率為31%,8%的受試者因藥物相關的不良事件停止用藥。
89例可評估的Claudin 18.2陽性胃癌或胃食管結合部腺癌患者在三個劑量組的確認的客觀緩解率(ORR)為33%,確認的疾病控制率(DCR)為70%。其中,2.2mg/kg劑量組確認的ORR為42%,中位無進展生存期(mPFS)為4.8個月,中位總生存期(mOS)尚未達到。
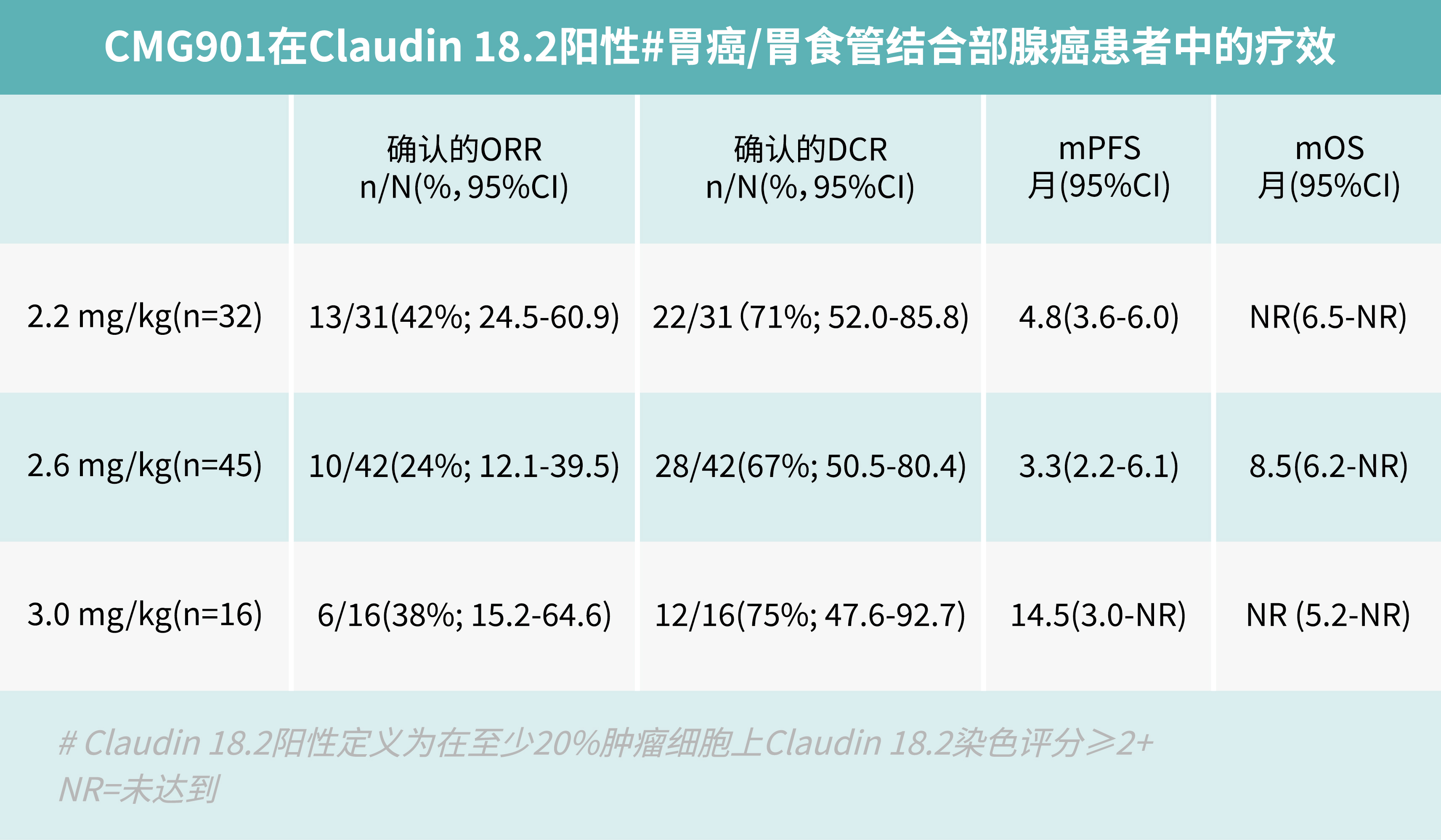
本次研究中,CMG901表現出了良好的安全性和耐受性,絕大部分不良事件在處理后可繼續用藥。CMG901在治療晚期Claudin18.2陽性胃癌╱胃食管結合部腺癌患者中表現出了優秀的療效。
