18周EASI-75應答率達73.9%!司普奇拜單抗青少年特應性皮炎III期臨床數據重磅亮相EADV 2025!
產品資訊
?2025年09月22日
2025年9月17-20日,第34屆歐洲皮膚病與性病學會(EADV)大會在法國巴黎舉行,本屆大會上,由北京大學人民醫院張建中教授團隊牽頭的一項多中心、隨機、雙盲、安慰劑對照Ⅲ期臨床研究(NCT06277765)公布了最新成果1,該研究聚焦于司普奇拜單抗治療青少年中重度特應性皮炎(AD)的療效與安全性,不僅為臨床實踐提供了新的循證證據,也為廣大青少年AD患者帶來了新的曙光。
01
從成人到青少年:
司普奇拜單抗再獲突破
司普奇拜單抗是一種全新人源化單克隆抗體,可精準靶向IL-4受體α亞基(IL-4Rα),同時阻斷 IL-4 和 IL-13 兩種關鍵細胞因子的信號傳導,從而有效緩解AD疾病癥狀2,3。與度普利尤單抗不同,司普奇拜單抗依賴空間表位與靶點結合,此表位與IL-4/IL-13結合位點鄰近甚至重合,繼而在阻斷IL-4Rα信號傳導方面表現更優4。目前,司普奇拜單抗已在中國獲批用于成人中重度AD的治療。盡管在成人群體中療效確切,但針對青少年AD患者的循證證據仍相對缺乏。因此,司普奇拜單抗用于青少年患者的Ⅲ期研究結果自啟動以來便備受學界與臨床關注。
該項Ⅲ期研究共納入180例12歲≤年齡<18歲的青少年患者,以2:1比例隨機分配至司普奇拜單抗組(n=120)或安慰劑組(n=60),雙盲治療周期為18周,并根據患者體重制定給藥方案(圖1)。共同主要終點設定為第18周時EASI評分較基線改善≥75%(EASI-75),以及IGA評分達到0或1分且較基線下降≥2分(IGA應答)。
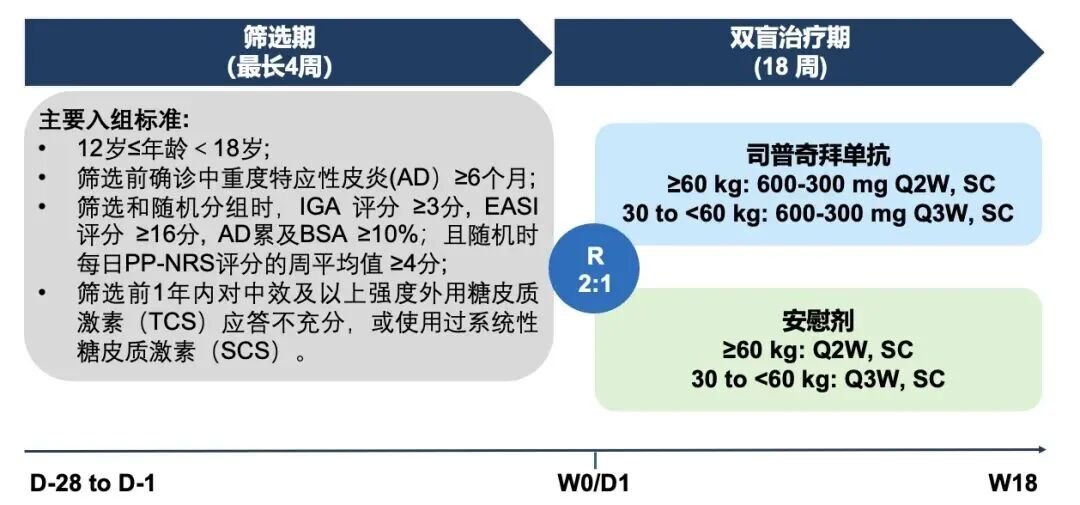
圖1:研究設計
02
主要終點均達到:
司普奇拜單抗顯著改善青少年患者皮損與瘙癢
治療第18周,司普奇拜單抗組達共同主要終點,均顯著優于安慰劑:
■ EASI-75應答率:18周時,司普奇拜單抗組高達73.9%的患者實現EASI-75應答,顯著高于安慰劑組(43.3%,P<0.0001)。(圖2A)
■ IGA應答率:18周時,司普奇拜單抗組IGA應答率高達 57.1%,顯著優于安慰劑組(25.0%,P<0.0001),進一步驗證了司普奇拜單抗在研究者整體評估中的療效優勢。(圖2B)
■ PP-NRS改善:司普奇拜單抗治療第18周,PP-NRS較基線改善高達49.5%。(圖2C)
上述結果一致表明,司普奇拜單抗在青少年中重度AD患者中同樣能夠實現強效的皮損改善與瘙癢緩解。
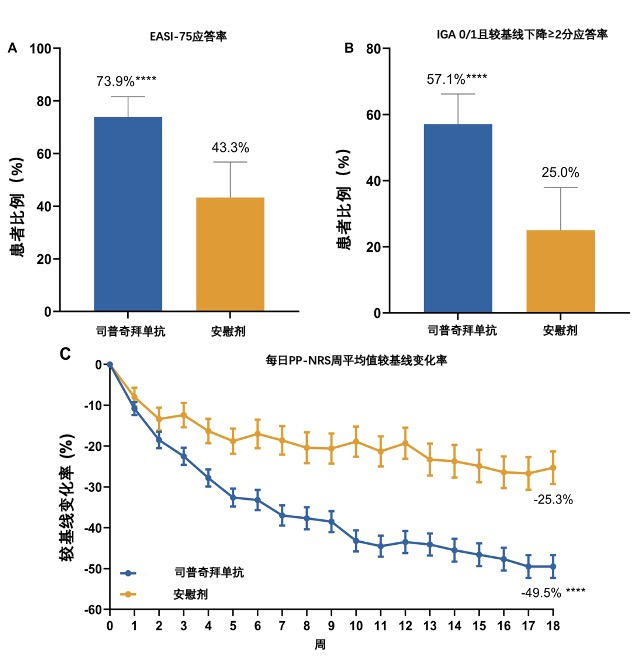
圖2:司普奇拜單抗治療18周患者改善:(A) EASI-75應答率;(B) IGA 0/1且較基線下降≥2分應答率;(C) 每日PP-NRS周平均值較基線變化率(****:P < 0.0001 vs. 安慰劑)
03
司普奇拜單抗
治療青少年AD安全性與耐受性良好
安全性方面,司普奇拜單抗組與安慰劑組的治療相關不良事件(TEAEs)發生率相當,且多為輕中度(表1)。最常見的不良事件為上呼吸道感染。值得關注的是,研究中未觀察到結膜炎不良事件的發生。這一結果提示,司普奇拜單抗不僅療效顯著,而且在青少年人群中具有良好的安全性與耐受性,為青少年AD患者提供新的更加安全可靠的治療選擇。
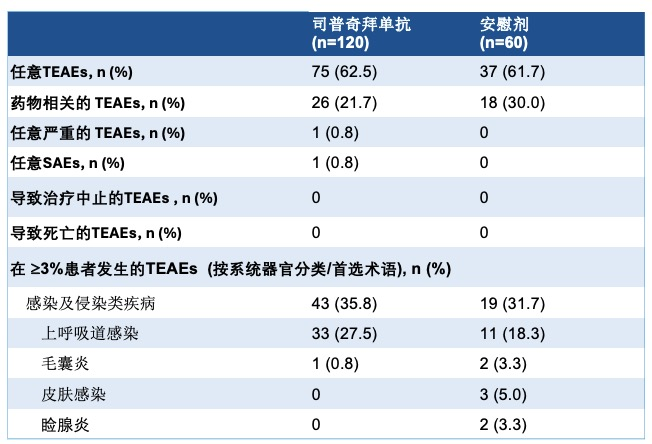
表1:安全性評估
本次EADV大會上公布的司普奇拜單抗青少年AD的Ⅲ期臨床數據顯示,司普奇拜單抗在青少年中重度特應性皮炎患者中展現出顯著的療效與良好的安全性,標志著該群體新型療法的一項重要進展。

張建中 教授
北京大學人民醫院皮膚科主任
“作為我國首個自主研發并成功獲批上市的IL-4Rα單抗,司普奇拜單抗在中重度特應性皮炎治療領域具有里程碑意義。本次EADV大會公布的青少年ADⅢ期臨床研究18周數據進一步印證了其強效改善及安全可控的優勢。期待未來積累更多真實世界研究和長期隨訪數據,為中重度AD的長期規范化管理提供更加堅實的循證支持。”
參考文獻:
1. Zhang J, Zhang F, Wei A, Zhou C, Zhao Y, Chen B, Huang Y, Liu W. Efficacy and safety of stapokibart in adolescents with moderate-to-severe atopic dermatitis: A phase 3 trial. Poster presented at: 34th European Academy of Dermatology and Venereology (EADV) Congress; 2025 Sep; Paris, France. Poster P3253.
2. Zhao Y, Zhang L, Zhang J; CM310AD005 Study Investigators. Efficacy and safety of stapokibart (CM310) in adults with moderate-to-severe atopic dermatitis: A multicenter, randomized, double-blind, placebo-controlled phase 3 trial. J Am Acad Dermatol. 2024;91(5):984-986. doi:10.1016/j.jaad.2024.07.1447.
3. Zhao Y, Zhang L, Wu L, et al. Long-term efficacy and safety of stapokibart for moderate-to-severe atopic dermatitis: 52-week results from a phase 3 trial. Allergy. 2025;80(5):1348-1357. doi:10.1111/all.16368.
4. Zhao Y, Zhang L, Wu L, et al. Stapokibart Rapidly and Consistently Improves the Clinical Signs Across All Body Regions in Adults With Moderate-to-Severe Atopic Dermatitis. Int J Dermatol. 2025;64(10):1939-1941. doi:10.1111/ijd.17820.
